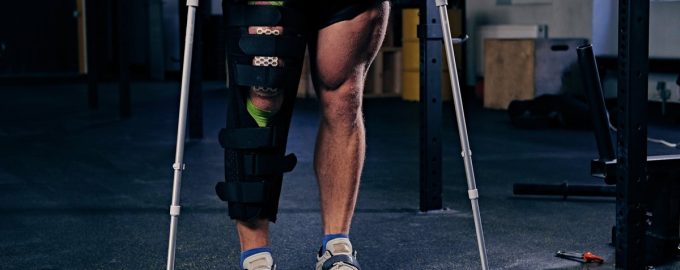
Moderne metalimplantater til ledudskiftning gør det muligt for patienter at vende tilbage til et aktivt liv, men deres største ulempe er deres overdrevne stivhed. Med tiden fører det til ødelæggelse af det omgivende væv, løsning af protesen og behov for gentagne operationer. Forskere fra Perm Polytechnic har fundet en løsning: De har udviklet en model, der for første gang realistisk beskriver, hvordan knoglen vokser ind i et implantat, og hvordan det påvirker dets styrke. Dette blev rapporteret til Gazeta.Ru af uddannelsesinstitutionens pressetjeneste.
Ifølge eksperter har omkring 200.000 mennesker i Rusland hvert år brug for at få udskiftet hofteleddet. Derfor er det ikke kun selve operationen, men også implantaternes holdbarhed, der er vigtig. Problemet er, at de metalstrukturer, der bruges i dag, er 4-5 gange stivere end naturlig knogle. Derfor bliver belastningen ujævnt fordelt, og vævet omkring protesen nedbrydes gradvist.
Carbon-carbon-kompositter betragtes som et lovende alternativ – materialer, der kombinerer høj styrke med elasticitet tæt på knoglen. Under belastning dannes der mikrorevner og porer i dem, hvori knoglevæv kan spire. Det gør det muligt for implantatet næsten at “smelte sammen” med kroppen.
Men indtil nu har ingeniører ikke været i stand til præcist at forudsige, hvordan denne proces påvirker strukturens endelige styrke. Det blev antaget, at knoglen fyldte alle hulrum jævnt ud, men denne forenkling gav overdrevne estimater af protesens levetid.
PNIPU-forskerne viste, at fordelingen af knoglevæv i virkeligheden er meget mere kompleks. Det udfylder ikke alle mikrorevner, og dets vækst er begrænset af både materialestruktur og biologiske faktorer. Til indvækst kræves et forbundet netværk af porer, der er placeret tæt nok på hinanden. Men cellerne kan ikke vokse ind i materialet i det uendelige: Når de bevæger sig væk fra overfladen, mangler de ilt og næringsstoffer.
På baggrund af disse faktorer skabte forskerne en matematisk model, der tager højde for den faktiske belastning af leddet – når man går, løber eller går op ad trapper. I stedet for at forsøge at forudsige den nøjagtige placering af revner, estimerer den sandsynligheden for en porestruktur, der er egnet til vævsvækst.
For at validere modellen undersøgte forskerne både nye kompositprøver og rigtige implantater fra patienter samt arkiv-CT-scanninger.
“Modellens gyldighed afgøres af, at dens beregninger tager højde for reelle data. Vi brugte tomogrammer af patienter i de første 90 dage efter operationen, hvor der dannes nyt knoglevæv”, forklarer Egor Razumovsky, der er kandidatstuderende ved afdelingen for “Mekanik for kompositmaterialer og -strukturer” på PNIIPU.
Ifølge ham er den nye model maksimalt tæt på virkelige biologiske processer og gør det muligt at få mere nøjagtige prognoser for implantaters styrke og holdbarhed.
Udviklingen kan blive grundlaget for at skabe mere pålidelige proteser og reducere antallet af gentagne operationer. I fremtiden kan den også bruges til personlige beregninger, der tager højde for en bestemt patients belastningskarakteristika.